基金投资企业复宏汉霖自主研发的H药再登国际权威期刊
近日,基金投资企业、国际化的创新生物制药公司复宏汉霖自主研发的抗PD-1单抗H药 汉斯状®(斯鲁利单抗)联合化疗一线治疗食管鳞状细胞癌(ESCC)的Ⅲ期临床研究(ASTRUM-007)结果在国际权威期刊Nature Medicine(影响因子:87.241)正式发表,该研究由国家癌症中心/国家肿瘤临床医学研究中心/中国医学科学院北京协和医学院肿瘤医院黄镜教授牵头开展。

ASTRUM-007研究结果已于2022年11月在中国临床肿瘤学会(CSCO)年会上以口头报告亮相,并于同年12月在欧洲肿瘤内科学会亚洲年会(ESMO Asia)上进行了口头报道。此次正式发表于Nature Medicine,再次在国际学术舞台展现了中国医药企业自主研制PD-1单抗的创新水平和研发实力。基于该研究结果,H药相关适应症的上市注册申请已经获国家药品监督管理局(NMPA)受理,并于近日获得《中国食管癌放射治疗指南(2022年版)》推荐与化疗联用一线治疗PD-L1 CPS≥1的晚期食管鳞癌。
食管癌是全球范围内十分常见的恶性肿瘤,主要分型为鳞状细胞癌和腺癌,84%以上属于食管鳞状细胞癌[1]。我国是食管癌高发地区,根据2016年中国恶性肿瘤发病率及死亡率估计,我国食管癌新发病例25.3万,死亡病例19.4万,发病率及死亡率分别位列恶性肿瘤的第6位和第5位[2]。由于早期食管癌症状往往不明显,大多数患者确诊时已处于临床中晚期,失去了手术治疗机会。目前临床对晚期患者主要采用系统治疗(化疗或靶向治疗),但治疗效果有限,复发率和转移率偏高。近年来,肿瘤免疫治疗已经成为国内外研究热点之一,多项研究表明抗PD-1单抗联合化疗可为食管癌患者带来生存获益,免疫检查点抑制剂联合化疗已成为我国食管癌的一线治疗标准[3]。
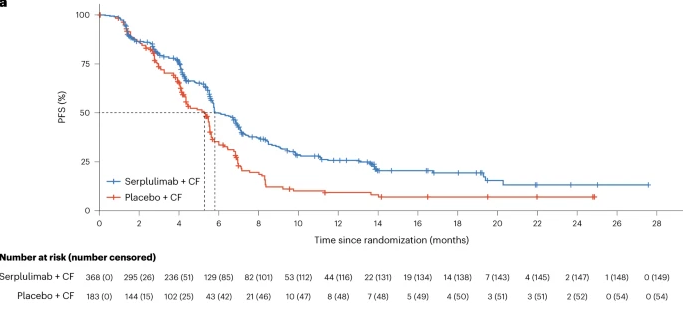
ASTRUM-007(NCT03958890)是一项随机、双盲、多中心的Ⅲ期临床试验,旨在研究斯鲁利单抗对比安慰剂分别联合化疗在既往未接受治疗、PD-L1阳性(综合阳性评分≥1)的晚期ESCC患者中的疗效和安全性。551例患者以2∶1的比例随机分组,两组患者分别接受斯鲁利单抗或安慰剂联合5-氟尿嘧啶和顺铂治疗(每2周1次)。斯鲁利单抗联合化疗组的中位无进展生存期(PFS)显著长于安慰剂联合化疗组(5.8 vs. 5.3个月;风险比[HR] 0.60,95% CI 0.48–0.75;p<0.0001)。斯鲁利单抗联合化疗组对比安慰剂联合化疗组的中位总生存期(OS)也获得了显著改善(15.3 vs. 11.8个月;HR 0.68,95% CI 0.53–0.87;p=0.0020)。安全性方面,斯鲁利单抗联合化疗的安全性良好。与单纯化疗相比,斯鲁利单抗联合化疗(每2周一次)作为一线治疗方案显著改善了PD-L1阳性晚期ESCC患者的PFS和OS,此治疗方案为该患者群体的治疗提供新选择。
H药 汉斯状®(斯鲁利单抗)是复宏汉霖首个自主研制的创新型单抗药。自2022年3月获批上市以来,H药已在中国获批用于治疗微卫星高度不稳定(MSI-H)实体瘤、鳞状非小细胞肺癌和广泛期小细胞肺癌(ES-SCLC),惠及逾10000名中国患者。以H药为基础,公司在全球开展多元化的肿瘤免疫联合疗法,并充分运用自有管线覆盖肿瘤特异性靶点、抗血管生成靶点和肿瘤免疫靶点等,助力H药与单抗、化疗等治疗手段开展联合治疗。以临床需求为导向,公司就H药在消化道肿瘤和肺癌领域进行了差异化、多维度布局,适应症广泛覆盖肺癌、肝细胞癌、食管鳞癌、头颈鳞癌和胃癌等高发大癌种,在全球范围内累计入组逾3100名受试者。
在消化道领域,H药已获批的MSI-H实体瘤适应症可为MSI-H高发的结直肠癌和胃癌等患者带去福音。此外,H药在胃癌新辅助/辅助方面也已达到临床研究III期,目前针对该细分领域的研究较少,公司在这一细分领域上处于国际领先地位,有望使胃癌患者在前线便从肿瘤免疫疗法中获益。在肺癌领域,H药针对ES-SCLC适应症的ASTRUM-005研究在全球四大顶级医学期刊之一的《美国医学会杂志》(JAMA,影响因子 157.3)在线发表,成为全球首个登上JAMA主刊的小细胞肺癌免疫治疗临床研究。此外,H药已分别获得美国食品药品监督管理局(FDA)和欧盟委员会(EC)授予的孤儿药资格认定,并入选《2022 CSCO小细胞肺癌诊疗指南》作为ES-SCLC治疗推荐。





